R-αリポ酸の効能とS-αリポ酸の毒性に関する論文の要約と考察(7)
前回のシリーズの(6)では、(1)から(4)までの現在でも何知らず市販されているαリポ酸サプリメントに含まれるS-αリポ酸の毒性に関する研究報告を振り返り、なぜ、このような糖尿病などの疾患をもつ人々が死亡する危険性のある成分が厚労省によって認められたのか、なぜ、S-αリポ酸はこのような毒性を持つのか、これまでの研究報告と自社での検討で判ってきたことを紹介し、説明しました。
では、なぜ、天然体のR-αリポ酸と非天然体のS-αリポ酸を50%ずつ含むラセミ体の形で厚労省はαリポ酸を認可し、そもそもヒトの体の中で合成されて、生体内で利用されている有益なR-αリポ酸が機能性成分として認められなかったのでしょうか?
その理由はR-αリポ酸の安定性がラセミ体と比較して極端に低く、食品や製剤への応用が困難なためでした。
R-αリポ酸は、熱、光などの外部刺激を与えることにより急速に分解し、粘着性を有する不溶性ポリマー凝集物に変化します。また、この凝集物は摩擦熱、圧縮、低pH環境下でも生成しますので、サプリメントとしてのカプセルや錠剤を作る時だけでなく、摂取した後に胃を通過する際にも胃酸によって分解されてしまいます。
そのような状況の中、いち早く、毒性の強い非天然のS-αリポ酸を含有するラセミ体の危険性を問題視した米国では、ラセミ体ではなく、R-αリポ酸の安定性を改善したR-αリポ酸のナトリウム塩の利用が増えつつあります。
しかしながら、R-αリポ酸のナトリウム塩はR-αリポ酸に比較すれば安定性は向上しているものの、その安定性は十分であるとは言い難いものです。そこで、私たちの研究グループは、食品に利用可能な三種の天然型シクロデキストリンであるα-シクロデキストリン、β-シクロデキストリン、γ-シクロデキストリンを用いてR-αリポ酸の包接安定化を検討しました。
その結果、γ-シクロデキストリンが最もR-αリポ酸(RALA)の包接安定化に適していて、熱に対しても、そして、強い酸性下でも図1と図2で示すように、R-αリポ酸のナトリウム塩(NaRALA)よりもγ-シクロデキストリン包接体(RALA-γ-CD)の方が安定であり、しかもR-αリポ酸を100%安定化できることを確認したのでした。
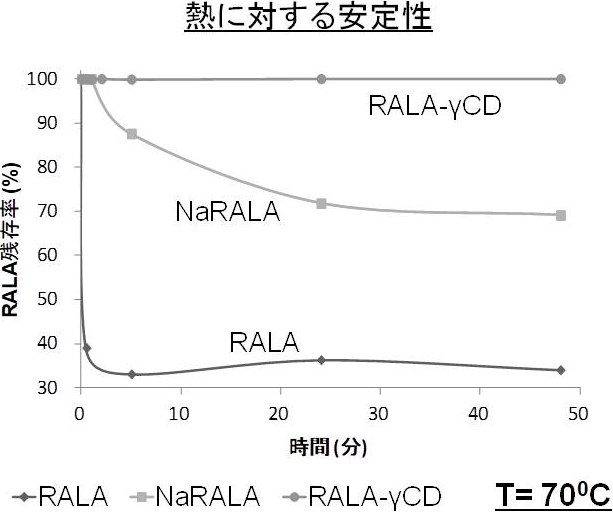
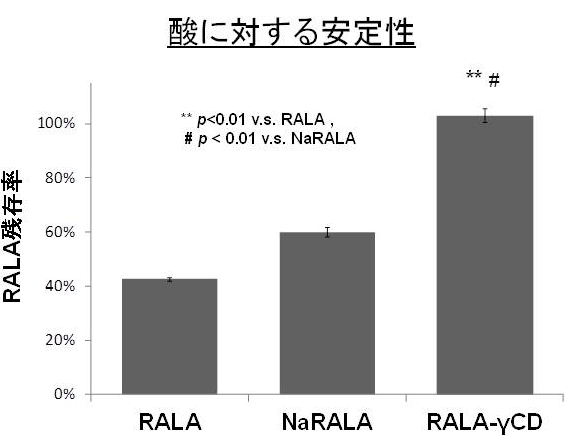
実際に、R-αリポ酸は胃酸のような強酸性水溶液中で不溶性ポリマー凝集物を形成していますが、 RALA-γ-CDは均一に分散することが確認できています。

そこで、さらに私たちは、安定性を高めたRALA-γ-CDを用いてヒト試験によるR-αリポ酸の生体利用能を検討しました。2群によるクロスオーバー試験を研究のデザインとし、健康な成人ボランティア6名(健常人、男性)を対象として3名ずつ、RALA単体、あるいはその包接体であるRALA-γ-CD(各600mgRALA相当)を水で経口投与しました。投与後、5、15、30、45、60、120、180分に肘静脈採血(各5mL)を行いました。尚、同意取得時に問診にて適格性を確認し、登録後、投与開始直前に血糖値を測定し、基準に満たない場合は中止としました。
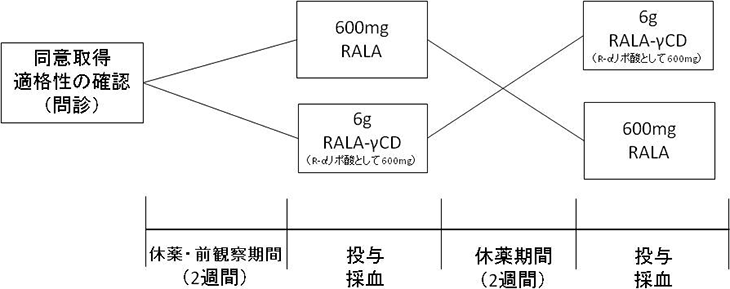
ヒト試験の結果、RALA-γ-CD経口投与による血中RALAのAUCとCmaxは未包接のRALAと比較し2.5倍であり、γ-CD包接化によって生体利用能が向上することを明らかとしました。
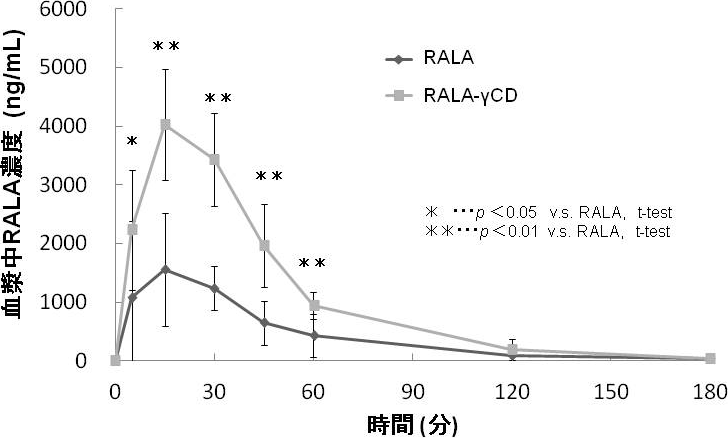
(6)でラセミ体のαリポ酸を経口摂取した論文を紹介しましたが、ラセミ体を摂取した場合にはR-αリポ酸もS-αリポ酸も吸収されますが、S-αリポ酸は血液中のアルブミンと反応して消失します。残りのR-αリポ酸の生体吸収率は胃酸に対して安定性が低いために3分の1以下です。
そこで、γ-CDで包接されていない市販されているαリポ酸ラセミ体のサプリメントとRALA-γ-CDを含有するサプリメントの吸収性の違いは……
2.5×2×3=15倍
の差があることになります。このように今では吸収性の高いR-αリポ酸のサプリメントが完成しているのです。
次回からは、R-αリポ酸の有益性について紹介したいと考えています。
